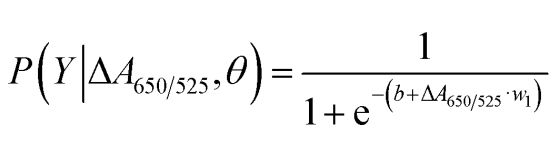Сұйық биопсияға негізделген қатерлі ісік ауруын ерте анықтау соңғы жылдары АҚШ-тың Ұлттық онкологиялық институты ұсынған қатерлі ісіктерді анықтау және диагностикалаудың жаңа бағыты болып табылады. Ол әртүрлі қатерлі ісіктерді, соның ішінде өкпе рагы, асқазан-ішек ісіктері, глиомалар және гинекологиялық ісіктерді ерте диагностикалау үшін жаңа биомаркер ретінде кеңінен қолданылды.
Метилдену ландшафтының (Methylscape) биомаркерлерін анықтауға арналған платформалардың пайда болуы науқастарды емдеуге болатын ең ерте сатыға қоя отырып, қатерлі ісікке ерте скринингті айтарлықтай жақсартуға мүмкіндік береді.
Жақында зерттеушілер цистеаминмен безендірілген алтын нанобөлшектеріне (Cyst/AuNPs) негізделген метилдену ландшафтын анықтауға арналған қарапайым және тікелей зондтау платформасын жасап шығарды, ол смартфон негізіндегі биосенсормен біріктіріліп, ісіктердің кең ауқымын жылдам ерте скринингке мүмкіндік береді. Лейкоздың ерте скринингін қан үлгісінен ДНҚ экстракциясынан кейін 90,0% дәлдікпен 15 минут ішінде жүргізуге болады. Мақаланың тақырыбы - цистеаминмен қапталған AuNP және машиналық оқыту мүмкіндігі бар смартфон арқылы адам қанындағы қатерлі ісік ДНҚ-сын жылдам анықтау.
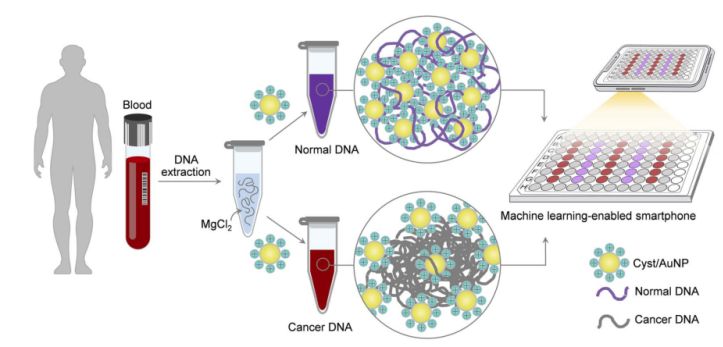
Сурет 1. Cyst/AuNPs компоненттері арқылы қатерлі ісік скринингі үшін қарапайым және жылдам зондтау платформасын екі қарапайым қадаммен орындауға болады.
Бұл 1-суретте көрсетілген. Алдымен ДНҚ фрагменттерін еріту үшін сулы ерітінді қолданылды. Содан кейін аралас ерітіндіге киста/AuNP қосылды. Қалыпты және қатерлі ДНҚ әртүрлі метилдену қасиеттеріне ие, нәтижесінде ДНҚ фрагменттері әртүрлі өзіндік құрастыру үлгілері бар. Қалыпты ДНҚ бос жиналып, ақырында Cyst/AuNPs біріктіреді, бұл Cyst/AuNPs қызылға ығысқан табиғатына әкеледі, осылайша түстің қызылдан күлгінге өзгеруін жалаң көзбен байқауға болады. Керісінше, қатерлі ісік ДНҚ-ның бірегей метилдену профилі ДНҚ фрагменттерінің үлкен кластерлерін өндіруге әкеледі.
96 шұңқырлы тақталардың суреттері смартфон камерасы арқылы түсірілді. Қатерлі ісік ДНҚ-сы спектроскопияға негізделген әдістермен салыстырғанда машиналық оқытумен жабдықталған смартфон арқылы өлшенді.
Нақты қан үлгілерінде қатерлі ісік скринингі
Сенсорлық платформаның пайдалылығын кеңейту үшін зерттеушілер нақты қан үлгілеріндегі қалыпты және қатерлі ДНҚ-ны сәтті ажырататын сенсорды қолданды. CpG сайттарындағы метилдену үлгілері ген экспрессиясын эпигенетикалық түрде реттейді. Қатерлі ісіктің барлық дерлік түрлерінде ДНҚ метилденуіндегі және осылайша ісік пайда болуына ықпал ететін гендердің экспрессиясындағы өзгерістердің ауысуы байқалды.
ДНҚ метилденуімен байланысты басқа ісіктердің үлгісі ретінде зерттеушілер лейкозбен ауыратын науқастардың қан үлгілерін және лейкозды ісіктерді саралаудағы метилдену ландшафтының тиімділігін зерттеу үшін сау бақылаушыларды пайдаланды. Бұл метилдену ландшафты биомаркері лейкозды скринингтің қолданыстағы жылдам әдістерінен асып түсіп қана қоймайды, сонымен қатар осы қарапайым және қарапайым талдауды қолдана отырып, қатерлі ісіктердің кең ауқымын ерте анықтауға дейін кеңейтудің орындылығын көрсетеді.
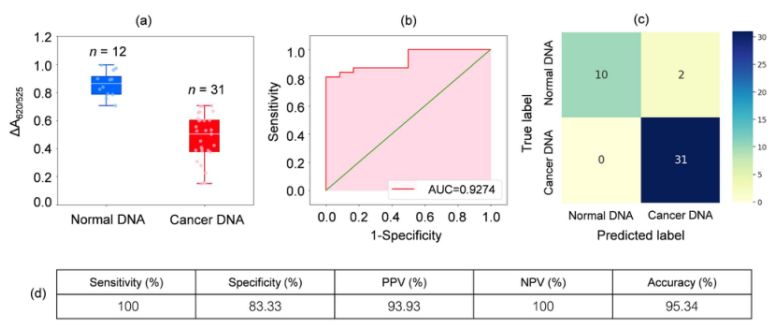
31 лейкозбен ауыратын және 12 сау адамның қан үлгілерінен алынған ДНҚ талданды. 2а суретіндегі қорап сызбасында көрсетілгендей, қатерлі ісік үлгілерінің салыстырмалы жұтылуы (ΔA650/525) қалыпты үлгілердегі ДНҚ-ға қарағанда төмен болды. бұл негізінен рак ДНҚ-ның тығыз агрегациясына әкелетін күшейтілген гидрофобтылыққа байланысты болды, бұл Cyst/AuNPs агрегациясын болдырмайды. Нәтижесінде, бұл нанобөлшектер қатерлі ісік агрегаттарының сыртқы қабаттарында толығымен дисперсті болды, бұл қалыпты және рак ДНҚ агрегаттарында адсорбцияланған Cyst/AuNPs әртүрлі дисперсиясына әкелді. Содан кейін ΔA650/525 ең төменгі мәннен максималды мәнге дейін шекті өзгерту арқылы ROC қисықтары жасалды.
Сурет 2.(a) оңтайландырылған жағдайларда қалыпты (көк) және қатерлі ісік (қызыл) ДНҚ бар екенін көрсететін киста/AuNPs ерітінділерінің салыстырмалы сіңіру мәндері
(DA650/525) қорап учаскелерінің; (b) ROC талдауы және диагностикалық сынақтарды бағалау. (c) Қалыпты және онкологиялық науқастарды диагностикалауға арналған шатастыру матрицасы. (d) әзірленген әдістің сезімталдығы, ерекшелігі, оң болжамдық мәні (PPV), теріс болжамдық мәні (NPV) және дәлдігі.
2b-суретте көрсетілгендей, әзірленген сенсор үшін алынған ROC қисығы астындағы аудан (AUC = 0,9274) жоғары сезімталдық пен ерекшелікті көрсетті. Қорап сызбасынан көрініп тұрғандай, қалыпты ДНҚ тобын білдіретін ең төменгі нүкте рак ДНҚ тобын білдіретін ең жоғары нүктеден жақсы ажыратылмаған; сондықтан қалыпты және қатерлі ісік топтарын ажырату үшін логистикалық регрессия қолданылды. Тәуелсіз айнымалылар жиынтығын ескере отырып, ол қатерлі ісік немесе қалыпты топ сияқты оқиғаның орын алу ықтималдығын бағалайды. Тәуелді айнымалы 0 мен 1 аралығында болады. Демек, нәтиже ықтималдық болып табылады. Біз ΔA650/525 негізінде қатерлі ісік идентификациясының ықтималдығын (P) төмендегідей анықтадық.
мұндағы b=5,3533,w1=-6,965. Үлгіні жіктеу үшін 0,5-тен төмен ықтималдық қалыпты үлгіні көрсетеді, ал 0,5 немесе одан жоғары ықтималдық қатерлі ісік үлгісін көрсетеді. 2c-суретте классификация әдісінің тұрақтылығын тексеру үшін пайдаланылған жалғыз қалдыру кросс-валидациядан жасалған шатасу матрицасы бейнеленген. 2d суретте сезімталдықты, ерекшелікті, оң болжамды мәнді (PPV) және теріс болжау мәнін (NPV) қоса алғанда, әдістің диагностикалық сынағының бағасы жинақталған.
Смартфонға негізделген биосенсорлар
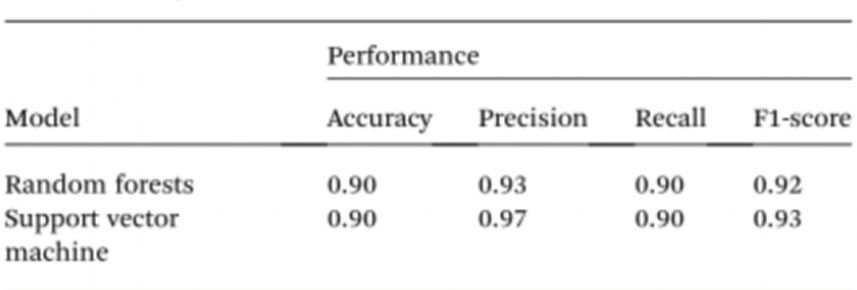
Спектрофотометрлерді қолданбай үлгілерді сынауды одан әрі жеңілдету үшін зерттеушілер ерітіндінің түсін түсіндіру және қалыпты және қатерлі ісік адамдарын ажырату үшін жасанды интеллектті (AI) пайдаланды. Осыны ескере отырып, ұялы телефон камерасы арқылы алынған 96 шұңқырлы пластиналардың кескіндерін пайдаланып, Cyst/AuNPs ерітіндісінің түсін қалыпты ДНҚ (күлгін) немесе қатерлі ісік ДНҚ (қызыл) түріне аудару үшін компьютерлік көру қолданылды. Жасанды интеллект смартфонның кез келген оптикалық аппараттық аксессуарларын қолданбай-ақ, шығындарды азайтып, нанобөлшектік шешімдердің түсін түсіндірудің қолжетімділігін жақсарта алады. Соңында, екі машиналық оқыту моделі, соның ішінде Random Forest (RF) және Support Vector Machine (SVM) үлгілерді құрастыру үшін оқытылды. RF және SVM үлгілері үлгілерді 90,0% дәлдікпен оң және теріс деп дұрыс жіктеді. Бұл ұялы телефон негізіндегі биосезімдеуде жасанды интеллектті пайдалану әбден мүмкін екенін көрсетеді.
Сурет 3.(a) Суретті алу қадамына үлгіні дайындау кезінде жазылған ерітіндінің мақсатты класы. (b) Кескінді алу қадамы кезінде алынған сурет үлгісі. (c) Суреттен алынған 96 шұңқырлы пластинаның әрбір ұңғымасындағы киста/AuNPs ерітіндісінің түс қарқындылығы (b).
Cyst/AuNPs көмегімен зерттеушілер лейкозды скрининг үшін нақты қан үлгілерін пайдаланған кезде метилдену ландшафтын анықтауға арналған қарапайым зондтау платформасын және қалыпты ДНҚ-ны рак ДНҚ-сынан ажырата алатын сенсорды сәтті әзірледі. Әзірленген сенсор нақты қан үлгілерінен алынған ДНҚ лейкозбен ауыратын науқастарда онкологиялық ДНҚ-ның аз мөлшерін (3nM) 15 минут ішінде жылдам және үнемді анықтай алатынын көрсетті және 95,3% дәлдік көрсетті. Спектрофотометрдің қажеттілігін жою арқылы үлгіні сынауды одан әрі жеңілдету үшін ұялы телефон фотосуреті арқылы ерітіндінің түсін түсіндіру және қалыпты және қатерлі ісік ауруына шалдыққан адамдарды ажырату үшін машиналық оқыту қолданылды, сонымен қатар дәлдік 90,0% деңгейінде қол жеткізілді.
Анықтама: DOI: 10.1039/d2ra05725e
Жіберу уақыты: 18 ақпан 2023 ж
 中文网站
中文网站